近几十年来,多种肿瘤治疗策略已经被开发和使用,但由于癌细胞的自我保护机制——自噬的存在,它们的治疗效果并不完全理想。自噬是一种高度保守且复杂的细胞内降解过程,在肿瘤发生和肿瘤治疗中起着关键作用,其中活性氧(ROS)的过度产生被认为是保护性自噬激活的直接原因。只有少数药物被用作肿瘤治疗中的自噬抑制剂,以减轻保护性自噬。其中,羟氯喹(HCQ)作为临床上最常用的自噬抑制剂,存在治疗剂量高、毒性大、非特异性作用显著等诸多问题。因此,通过自噬抑制实现肿瘤治疗仍然面临巨大的挑战。

针对这一问题,西安交通大学第一附属医院皮肤科郑焱教授团队与西北工业大学化学与化工学院瞿永泉教授团队合作,使用两步水热法合成纳米酶——多孔氧化铈纳米棒(PN-CeO2),并将其作为自噬抑制剂,通过催化清除ROS来抑制保护性自噬,从而实现肿瘤治疗。研究通过透射电子显微镜(TEM)、X射线能谱仪(EDS)、X射线衍射仪(XRD)、X射线光电子能谱(XPS)等对PN-CeO2进行了基本表征,并在体外对PN-CeO2的类超氧化物歧化酶(SOD)及类过氧化氢酶(CAT)活性进行了评估,从而验证了其抗氧化活性;进一步使用具有高自噬水平的皮肤鳞状细胞癌(cSCC)作为治疗的肿瘤模型,系统性地检验了PN-CeO2体内外的抗肿瘤活性、作用途径及其生物安全性。研究结果证实,PN-CeO2纳米酶作为自噬抑制剂,可以通过其特殊的抗氧化酶模拟活性,高效催化降解肿瘤内的ROS,进一步抑制cSCC中PI3K/AKT和p38MAPK通路的激活来抑制保护性自噬并激活凋亡,最终实现高效的肿瘤杀伤作用(图1)。此外,该研究强调,相较于毒性作用显著的HCQ,PN-CeO2是一种安全有效的抗肿瘤自噬抑制剂。总之,该研究提出了一种还原性损伤策略,作为一种有前途的抗肿瘤方法,它可以通过催化降解ROS来抑制保护性自噬,从而为肿瘤治疗提供了引人注目的新思路。
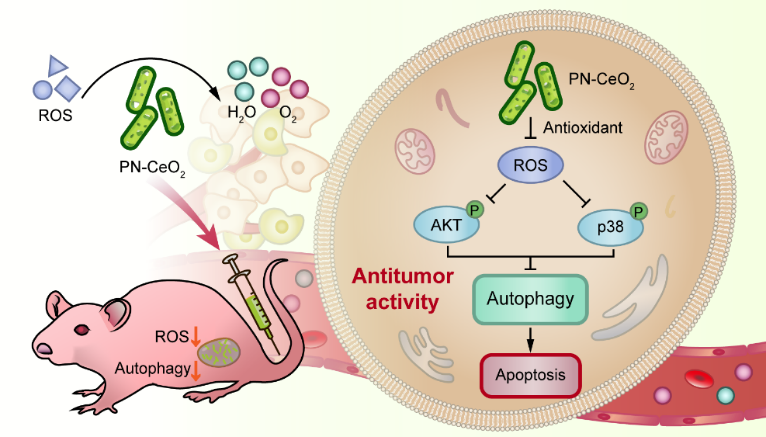
图1 PN-CeO2通过还原性损伤诱导自噬抑制的肿瘤治疗机制图
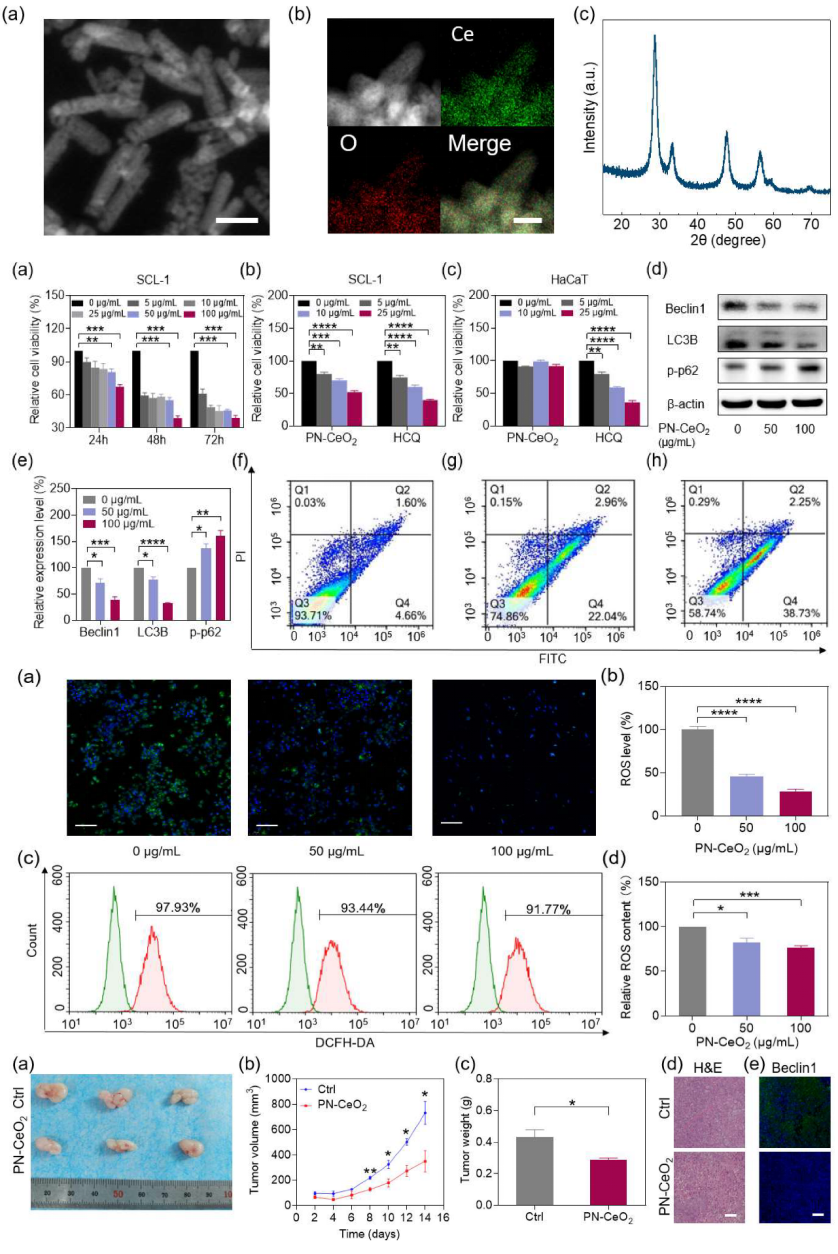
图2 PN-CeO2的结构表征及cSCC治疗作用
该文章近期在线发表在NanoResearch(IF=10.269)上,题目为“Reductive damage induced autophagy inhibition for tumor therapy”。西安交通大学第一附属医院为该论文第一作者和第一通讯作者单位,西安交通大学第一附属医院皮肤科郑焱教授、西北工业大学瞿永泉教授及田志敏博士为该论文的共同通讯作者,博士生王玉倩和黄英剑博士为该论文的共同第一作者。NanoResearch期刊2021年影响因子为10.269,并在纳米科学、纳米技术,应用物理学,化学、物理,材料科学、多学科等多个领域位于JCR一区。
论文链接
https://link.springer.com/article/10.1007/s12274-022-5139-z
